Ny viden: Trojansk hest kan hjælpe medicin forbi hjernens forsvarsværk
Blod-hjerne-barrieren beskytter hjernen og er notorisk svær for lægemidler at komme forbi, og det gør det vanskeligt at behandle lidelser i centralnervesystemet. I et muse-studie anvendte et forskerhold fra Københavns Universitet en ny tilgang til at undersøge barrieren og hjælpe med at snige lægemidler forbi den ved hjælp af en teknik inspireret af den trojanske hest.
Sklerose, Parkinsons, Alzheimers og epilepsi er blot nogle få af de lidelser, man kan få i centralnervesystemet. Sygdommene er meget vanskelige at behandle, da hjernen er beskyttet af blod-hjerne-barrieren.
Blod-hjerne-barrieren fungerer som et forsvarsværk mellem blodet og hjernen, så kun bestemte molekyler kan trænge ind i hjernen. Vand og ilt godt kan godt komme igennem på samme måde som andre stoffer såsom alkohol og kaffe, men muren forhindrer mere end 99 procent af de potentielt neurobeskyttende elementer i at nå deres mål i hjernen.
I et studie udført med levende, vågne mus, giver et forskerhold fra Københavns Universitet nu direkte indsigt i, hvordan man kan snyde blod-hjerne-barrierens uigennemtrængelige mur og gøre det muligt at frigive lægemidler til hjernen.
De undersøgte de såkaldte nanopartikel-liposom som lægemiddelbærere og fik dem sneget forbi blod-hjerne-barrieren, samtidig med at de sporede og overvågede dem hele vejen gennem systemet.
”Før dette studie havde man ingen indsigt i, hvad der skete ved blod-hjerne-barrieren i den levende hjerne, og specielt hvorfor nogle nanopartikler kunne krydse over, mens andre ikke kunne. Blod-hjerne-barrieren en ’sort boks’ i den sammenhæng, hvor samspillet mellem lægemiddelindgift og sporing i hjernen var uklar. Der var endda tvivl om, hvorvidt nanopartikler overhovedet kunne trænge ind i hjernen. Vores studie giver nu direkte bevis for, at nanopartikler kan trænge ind i hjernen, og beskriver, hvorfor, hvornår og hvor det sker,” forklarer adjunkt Krzysztof Kucharz fra Institut for Neurovidenskab.
Analogt til mytens trojanske hest snyder nanopartiklerne endotelium, det vil sige hovedkomponenten i blod-hjerne-barrieren, så de kan optages og transporteres gennem blod-hjerne-barrieren til hjernen.
Med hjælp fra kolleger ved Danmarks Tekniske Universitet og Aalborg Universitet brugte forskerne to-foton-billeddannelse til at dekonstruere blod-hjerne-barrieren for at forstå, hvordan nanopartikler som lægemiddelbærerne trænger gennem blod-hjerne-barrieren i en levende organisme.
”Vi overvågede nanopartiklens adgang til hjernen i forbindelse med alle trin i processen, hvilket gav os værdifuld viden til brug for fremtidens lægemiddeldesign. Specifikt viser vi, hvilke vaskulære segmenter nanopartiklerne mest effektivt kan rettes mod for at sikre, at de kommer ind i hjernen. Og fordi vi var i stand til at overvåge lægemiddelbærerne helt nede på niveau med en enkelt nanopartikel, har vi nu en ny platform til at udvikle mere effektive og sikrere terapeutiske tilgange,” siger Krzysztof Kucharz.
Brug af en trojansk hest
Studiet, der er offentliggjort i Nature Communications, viser, at nanopartikler, der er målrettet mod hjernen, opsamles i kapillærerne og venolerne af endotelceller, som er de celler i blod-hjerne-barrieren, der tillader eller afviser molekylers adgang til hjernevævet.
”Analogt til mytens trojanske hest snyder nanopartiklerne endotelium, det vil sige hovedkomponenten i blod-hjerne-barrieren, så de kan optages og transporteres gennem blod-hjerne-barrieren til hjernen. Nanopartikler har et lastrum, der kan fyldes med forskellige neurobeskyttende lægemidler til behandling af mange neurodegenerative sygdomme. Denne tilgang efterprøves for tiden i adskillige kliniske og prækliniske forsøg med hjernecancer, slagtilfælde, Alzheimers og Parkinsons. Dog er niveauerne for transport af nanopartikler ind i hjernen stadig lave og skal forbedres for få klinisk betydning. Der er et stort behov for at optimere lægemiddelafgivelsen ved hjælp af nanopartikler, men for at kunne gøre det, er det nødvendigt at forstå, hvordan nanopartikler interagerer med blod-hjerne-barrieren i den levende hjerne. Det er i den forbindelse, vi kom på banen,” siger Krzysztof Kucharz.
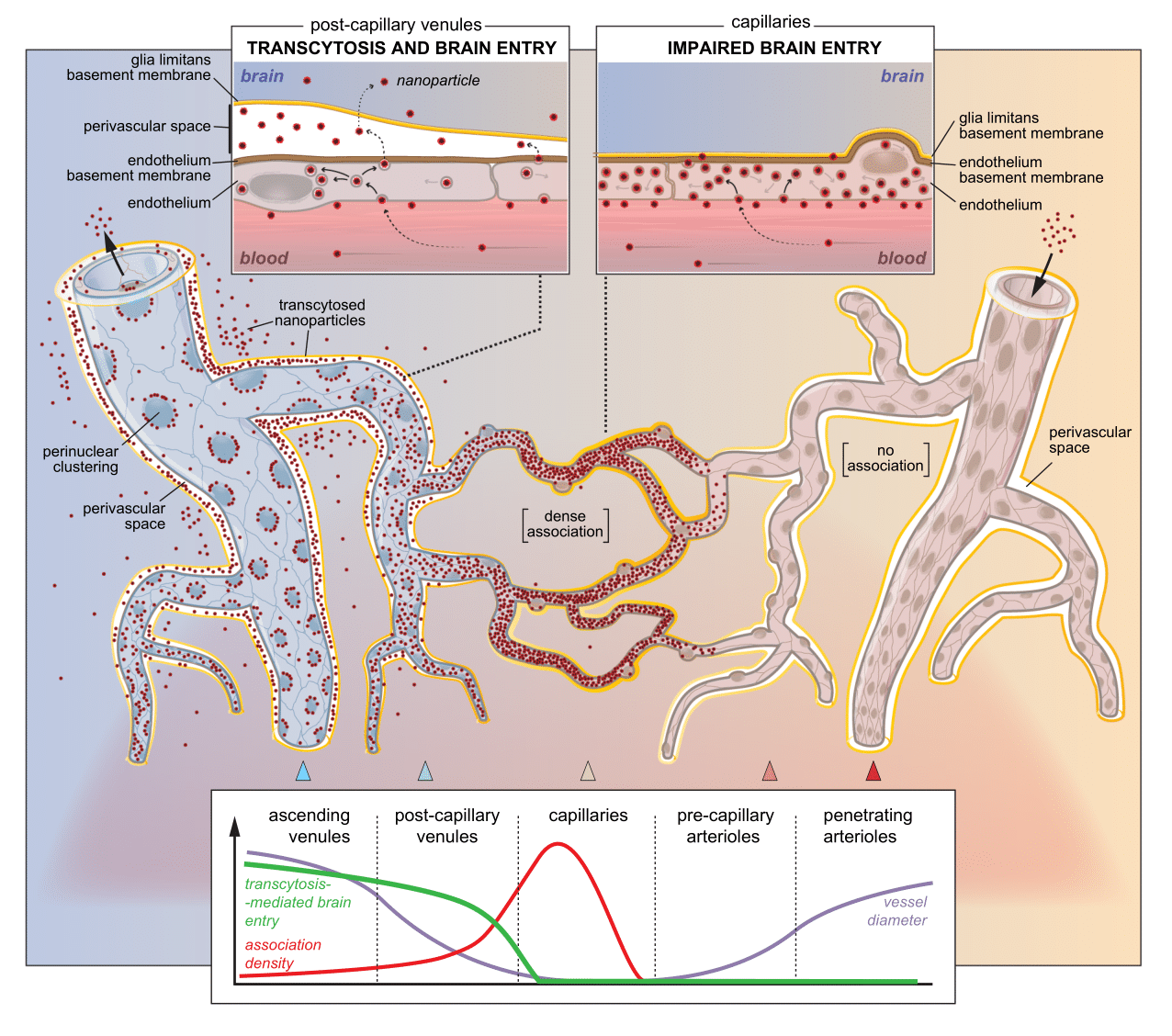
De viser, at nanopartikler kan trænge ind i hjernen på tværs af venoler, det vil sige store kar, som er omgivet af såkaldte perivaskulære rum, og ikke, som tidligere antaget, på tværs af små og talrige kapillærer. Det perivaskulære rum omgiver venolerne, hvilket gør det nemmere for nanopartikler at komme ud af endotelium og trænge længere ind i hjernen, men dette rum eksisterer ikke i kapillærer.
”Vores resultater udfordrer den gængse opfattelse af, at kapillærer er det vigtigste område for transport af nanopartikler til hjernen. I stedet skal arbejdet med at opnå en effektiv lægemiddeltilførsel til hjernen ved hjælp af nanopartikler koncentreres om venolerne,” siger Krzysztof Kucharz.
Et stort skridt fremad i behandlingen af hjernesygdomme
Forskerne brugte to-foton-billeddannelse til at studere fluoresceret-mærkede nanopartikler, hvilket tillod dem at åbne blod-hjerne-barrierens ”sorte boks” og få et fuldstændigt billede af nanopartiklernes skæbne i takt med, at de trængte gennem blod-hjerne-barrieren til hjernen.
Nu kunne de observere, hvordan nanopartikler cirkulerer i blodbanen, hvordan de over tid binder sig til endotelium, hvor mange der optages i endotelium, hvor mange der er tilbage, hvad der sker med dem, når de først er inde i blod-hjerne-barrieren, og hvor nanopartiklerne forlader hjernen. Derefter opdagede de, at hjernens kar håndterer nanopartiklerne forskelligt og tillader eller nægter dem adgang til hjernevævet, afhængigt af typen af kar.
"Selvom anatomien og funktionen af endotelium er forskellig for forskellige kartyper, så var dette karakteristikum i hjernen blevet overset i tidligere undersøgelser af lægemiddelafgivelse, og om eller hvordan det påvirkede lægemiddelafgivelse har hidtil været ukendt,” siger Krzysztof Kucharz.
Den metodologiske platform, der er udviklet af forfattere, skal nu afprøves i Martin Lauritzens laboratorium med henblik på finjustering af nanopartikeltransporten og for finde ud af, hvordan blod-hjerne-barrierens egenskaber er forskellige i syge og aldrende hjerner. Dette vil forhåbentligt betyde det næste stort skridt fremad i forbindelse med behandlingen af hjernesygdomme.
Kontakt
Adjunkt Krzysztof Kucharz
kucharz@sund.ku.dk
+45 51 19 14 87
Professor Martin Lauritzen
mlauritz@sund.ku.dk
+45 24 84 18 40
Journalist Søren Thiesen
s.thiesen@sund.ku.dk
+45 28 75 29 34
