Nyt studie: Parkinsons sygdom skyldes nedbrud i cellens kraftværk
En ny undersøgelse afslører, at hovedårsagen til Parkinsons sygdom er en fejlregulering af de immungener, der er centrale for bekæmpelsen af vira. Forskere fra Københavns Universitet påviser, at fejlreguleringen fører til en funktionsfejl i cellens kraftværk, som dermed ikke kan producere tilstrækkeligt med energi til, at hjernecellerne kan holde sig i live, hvorefter de begynder at dø.

12.000 mennesker i Danmark og mellem syv til ti millioner mennesker på verdensplan over lider af Parkinsons sygdom (PS). Det er den næstmest almindelige neurogenerative aldringslidelse og den mest almindelige bevægelseslidelse, men årsagen til sygdommen er stort set ukendt.
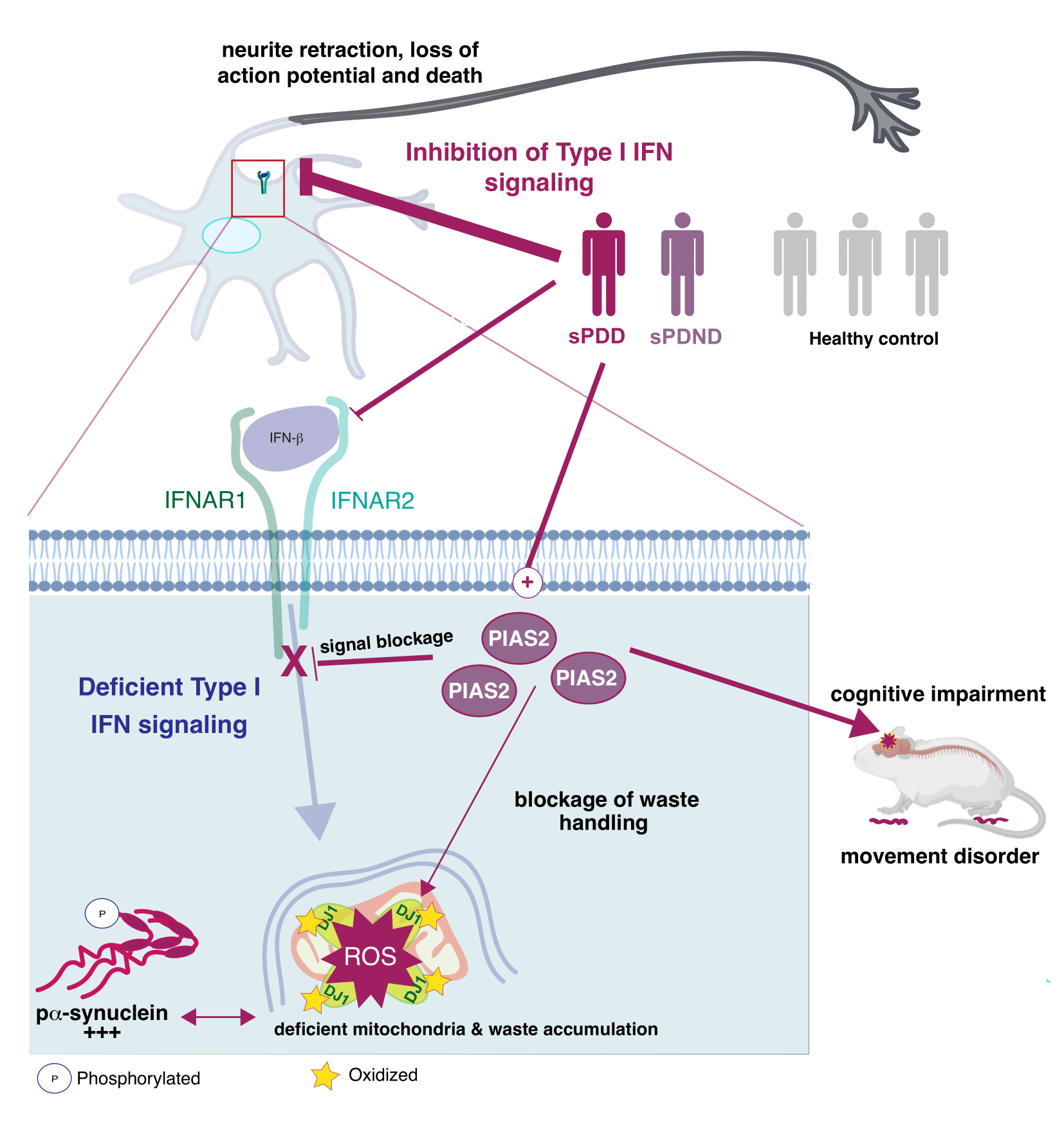
I en ny undersøgelse viser forskere fra Københavns Universitet, at sporadisk PS - den mest almindelige form af sygdommen, der omfatter 90 til 95 procent af alle Parkinsons sygdomstilfælde - skyldes en signalblokering af en sti, der regulerer nervecellens kraftværk, mitokondrierne.
”Ligesom når folk spiser, tager cellerne det, de har brug for, og skiller sig af med affaldsprodukterne. Men hvis vores hjerneceller har denne specifikke form for signalblokering, så betyder det, at cellens kraftværk – mitokondrierne – ikke kan blive renset efter at være blevet beskadiget,” forklarer studiets hovedforfatter og gruppeleder professor Shohreh Issazadeh-Navikas ved Biotech Research & Innovation Centre.
Blokeringen fører til en ophobning af store mængder beskadigede mitokondrier, samtidig med at der ikke kan produceres nok energi til cellerne. Det får neuronerne til gradvist at dø, og det er grunden til, at man udvikler symptomer på Parkinsons, og det er også grunden til, at det medfører demens.
Blokeringen er forårsaget af en fejlregulering af immungenerne. Konkret er det en såkaldt sti kaldet type 1-interferon, som også er vigtig i bekæmpelsen af virus. Nu viser forskerne så, at den også er ansvarlig for regulering af nervecellernes energiforsyning.
”Enhver del af vores krop skal reguleres. Når vi spiser og bliver mætte, får vi et signal om at holde op med at spise. Det samme sker overalt i vores krop. Hvis vi får en infektion, er dele af vores krop nødt til at bekæmpe den og forhindre den i at replikere sig. Men når infektionen er væk, skal signalet om at bekæmpe den forsvinde. Dette arbejde skal udføres af et protein, der hedder PIAS2. Det sørger for at blokere type 1-interferon-stien, og når infektionen er overstået, skal blokeringen stoppe og vende tilbage til normaltilstanden. Men det ser ikke ud til at være tilfældet hos patienter med Parkinsons sygdom. Vi påviser også, at den her fejlregulering, som nævnt før, fører til en defekt i cellens energiforsyning,” siger Shohreh Issazadeh-Navikas.
Disse stier med signalstoffer er både meget vigtige for hjernefunktionerne, men de er også forbundet med mikrobiel og virusgenkendelse. For eksempel spiller de en meget stor rolle, når vores krop skal bekæmpe COVID-19, og det har vist sig, at en mutation i det associerede gen også kan forbindes med dødeligt udfald efter at være smittet med corona.
Kombinerede datasæt giver et bedre overblik
Forskerne kombinerede og analyserede fire datasæt, som undersøgte hjerneceller fra hjerner med Parkinsons sygdom, og hvilken type gener de udtrykker.
Derefter kiggede de på, hvilke genmønstre der var forstyrret hos patienter med Parkinsons sygdom, især hos dem, der også havde udviklet PS med demens.
For at kontrollere resultaterne blev de vigtigste fund i de kombinerede datasæt afprøvet i tre forskellige musemodeller. Det skete ved hjælp af en negativ regulator af type 1-interferon-stien, PIAS2-proteinet, der i patientundersøgelsen var blevet identificeret som et af de nøgleproteiner, der er knyttet til progressionen af Parkinsons sygdom og til demens.
”En stor ophobning af PIAS2-proteinet er årsagen til blokering af den sti, der skulle have aktiveret de processer, der er ansvarlige for at fjerne beskadiget protein- og mitokondrieaffald i hjernen,” forklarer Shohreh Issazadeh-Navikas.
”Akkumuleringen af beskadiget mitokondriemasse fører yderligere til en stigning i andre giftige proteiner. Når vi sammenligner patienter med raske mennesker på samme alder, men uden Parkinsons sygdom, kan vi se, at dette PIAS2-protein kommer stærkt til udtryk i neuronerne, og derfor bør denne sti blive evalueret for potentielle roller i de andre former for arvelig Parkinsons sygdom, som vi ikke har studeret her.”
Forskerne håber, at undersøgelsen vil føre til yderligere forskning i, hvordan man kan modvirke blokering af stien, hvilket kunne have gavnlig indvirkning på sygdommen og på forebyggelsen af demens.
I de næste studier vil Shohreh-gruppen undersøge, hvordan stien bidrager til neuronal homeostase og overlevelse, samt hvordan dens fejlregulering er årsag til neuronal celledød.
Læs hele undersøgelsen “PIAS2-mediated blockade of IFN-β signaling: a basis for sporadic Parkinson disease dementia“ her.
Kontakt
Professor Shohreh Issazadeh-Navikas
shohreh.issazadeh@bric.ku.dk
+45 35 32 56 49
Journalist Søren Thiesen
s.thiesen@sund.ku.dk
+45 28 75 29 34
